Come fa il cervello a collegare miliardi di cellule con precisione, senza errori di “cablaggio”, in modo che possiamo pensare, muoverci e percepire il mondo? Un team dell’Ohio State University ha appena identificato un meccanismo molecolare chiave che spiega come due tipi specifici di neuroni stabiliscono contatti precisi tra loro. La scoperta, pubblicata sulla rivista The Journal of Neuroscience, apre nuove opportunità per comprendere i disturbi neurologici e psichiatrici associati a difetti nella connettività cerebrale. In termini semplici, i ricercatori descrivono un sistema paragonabile a una “stretta di mano” molecolare, una sorta di password biologica che permette a una cellula di riconoscere esattamente l’altra prima di connettersi. Quando questo riconoscimento funziona correttamente, i circuiti cerebrali si organizzano in modo ordinato; quando fallisce, l’equilibrio del sistema può essere alterato.
La “stretta di mano” molecolare che regola i circuiti cerebrali
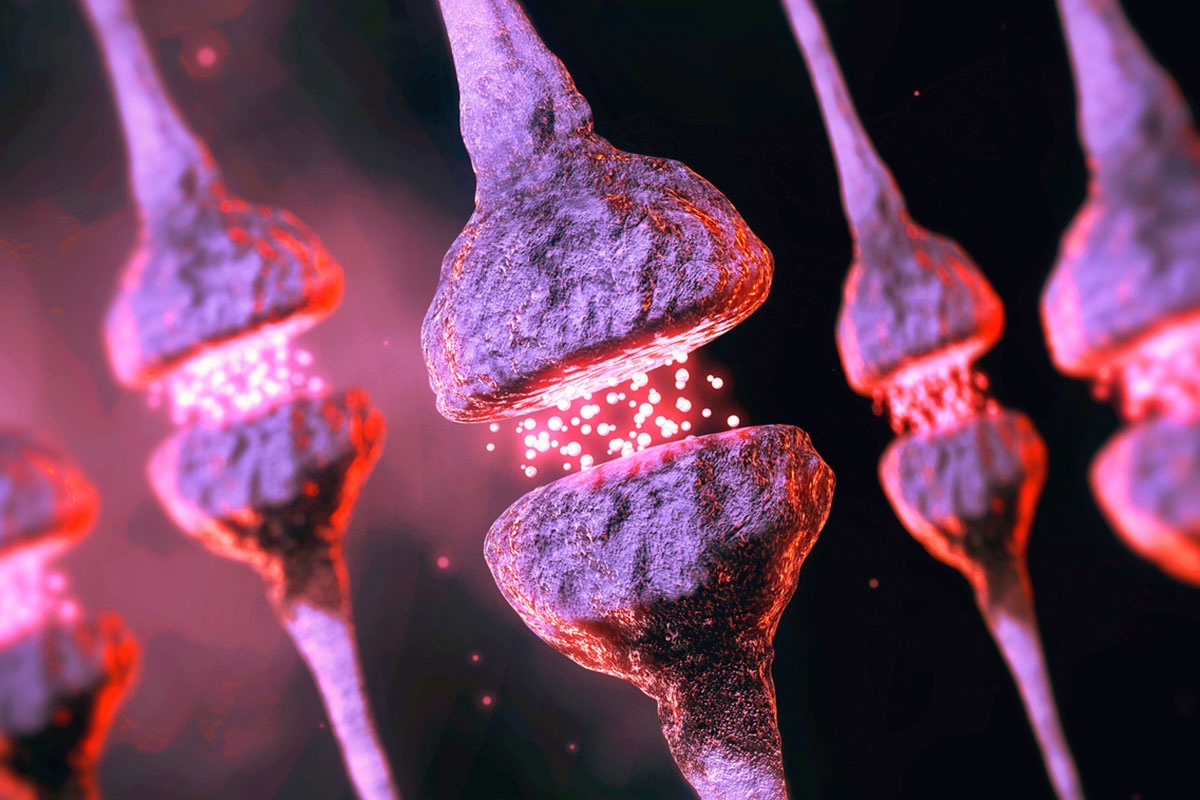
Lo studio si concentra sull’interazione tra proteine che rendono possibile la formazione di sinapsi, ovvero i punti di contatto tra i neuroni. Secondo Yasufumi Hayano, autore principale della ricerca, “questi interneuroni inibitori modellano e bilanciano l’attività del circuito locale; sono modulatori e coordinatori, i direttori d’orchestra”.
Le protagoniste della scoperta sono le cosiddette cellule chandelier, un tipo speciale di interneuroni inibitori. Sebbene siano poche, svolgono un ruolo decisivo: controllano l’attività dei neuroni piramidali, che sono responsabili della trasmissione dei segnali eccitatori e funzionano come una delle principali vie di uscita delle informazioni nel cervello.
Un modo semplice per immaginarlo è pensare a una città: i neuroni piramidali sarebbero le grandi strade dove circola il traffico principale, mentre le cellule chandelier agirebbero come i semafori che regolano il flusso per evitare incidenti e traffico. Senza questo controllo preciso, il sistema perde stabilità.
Il progresso fondamentale del team dell’Ohio State University è stato quello di identificare come le cellule chandelier riescono a connettersi sempre in un punto molto preciso dei neuroni piramidali: il segmento iniziale dell’assone, una regione chiave per decidere se il neurone si attiva o meno.
Questo contatto avviene grazie all’azione congiunta di tre proteine che operano come un sistema “chiave e serratura”. La gliomedina, presente nelle cellule chandelier, invia il segnale corretto; la CNTNAP4, sulla superficie cellulare, lo riconosce; e la Neurofascina-186, situata nell’assone, indica il punto preciso in cui deve avvenire l’incontro. Solo quando questi tre elementi si incastrano, la connessione si forma in modo stabile.
Negli esperimenti condotti sui topi, gli scienziati hanno osservato che, eliminando il gene della gliomedina, le cellule chandelier perdono la capacità di formare connessioni efficienti con i neuroni piramidali.
È come se una delle parti della “stretta di mano” scomparisse: l’identificazione fallisce e la connessione non si concretizza correttamente. L’università ha sottolineato che il riconoscimento reciproco tra queste tre molecole è indispensabile affinché i circuiti neuronali inibitori si sviluppino in modo adeguato.
Implicazioni nei disturbi neurologici e potenziale terapeutico
Uno degli aspetti più sorprendenti è l’influenza sproporzionata esercitata dalle cellule chandelier. Sebbene siano poche, agiscono come veri e propri regolatori del traffico cerebrale: regolano quando e come si attivano i neuroni piramidali, mantengono l’equilibrio tra eccitazione e inibizione e prevengono squilibri che potrebbero influenzare il normale funzionamento del cervello.
Secondo l’Ohio State University, alterazioni in questa “stretta di mano” molecolare sono state collegate all’epilessia, all’autismo, alla schizofrenia e alla depressione. In tutti questi casi, la perdita di coordinazione tra interneuroni inibitori e neuroni piramidali appare come un fattore comune.
Comprendere in modo più dettagliato come funziona questo meccanismo permette di studiare non solo cosa non funziona in questi casi, ma anche dove si potrebbe intervenire. Hiroki Taniguchi, ricercatore senior dello studio, ha sottolineato il potenziale terapeutico della scoperta. Secondo lo specialista, conoscere come si formano questi contatti specifici può facilitare lo sviluppo di trattamenti mirati a ripristinare i circuiti cerebrali alterati.
I risultati rafforzano l’importanza delle proteine gliomedina, CNTNAP4 e Neurofascina-186 nella costruzione di connessioni precise all’interno del cervello. Sulla base di questi risultati, il team ritiene possibile che future ricerche identifichino nuovi bersagli terapeutici per patologie neurologiche complesse.
Comprendere come il cervello stabilisce questo tipo di “accordi” molecolari è un primo passo per progettare strategie che consentano di correggere i difetti di connettività, un aspetto centrale in numerose malattie che colpiscono la funzione cerebrale.